Nano Res.[生物]│刺激响应开关-递送系统实现空间-时间精准性的钥匙
本篇文章版权为张飞黎佳祺所有,未经授权禁止转载。

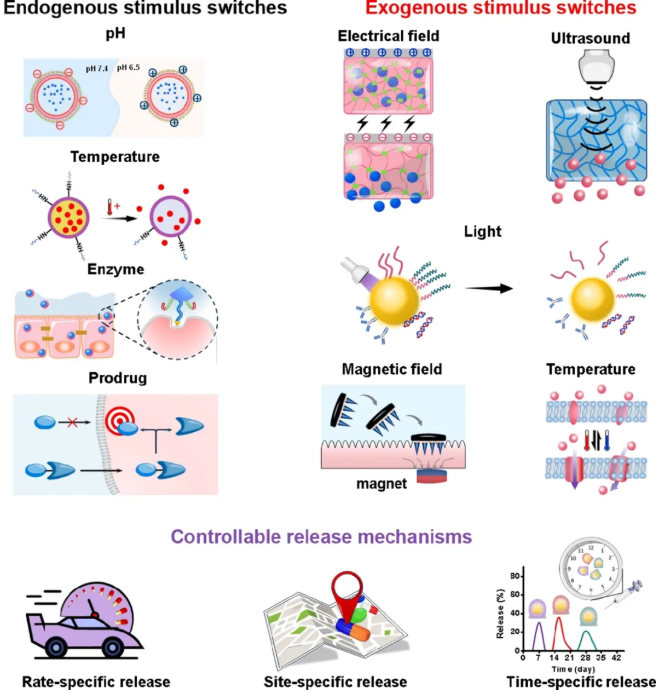
背景介绍 精准医疗的兴起为疾病治疗带来了革命性变化,其核心在于针对分子病理机制或特定微环境开发治疗剂,从而减少全身副作用并提升治疗效果。然而,当前的治疗手段在空间和时间控制上存在显著局限性,导致药物在非靶组织的富集,引发系统性副作用,影响患者愈后恢复。为此,刺激响应型药物递送系统应运而生,旨在通过精准调控药物释放的时空特性,克服现有治疗的不足。 本文综述了用于设计刺激开关的生物材料和分子释放机制,以实现治疗递送的时间、地点和速度精度,为改善患者的治疗效果,推动精准医疗向更深层次发展提供思路。 成果简介 用于精确治疗的特定触发释放机制示意图 内源性刺激开关 内源性刺激开关内源性刺激开关是精准治疗递送系统中的重要组成部分,其设计灵感来源于病理组织独特的微环境特征。肿瘤细胞外环境的pH值通常较低,介于6.5-7.2之间,研究者据此开发了pH响应性药物载体,这些载体在正常生理条件下保持稳定,而在肿瘤微环境中因pH值变化触发药物释放。同样,恶性肿瘤或炎症组织常伴随体温升高,温度敏感性聚合物可在此类环境中响应温度变化,实现药物的靶向递送。病理状态下的酶水平显著高于正常组织,研究者利用这一特点构建了酶响应型药物递送系统。含有二硫键和硒键的药物载体可在高还原环境的肿瘤细胞内快速释放药物。前药刺激开关通过化学修饰药物,使其在病理微环境中经酶促或非酶促转化后释放活性形式。这些内源性刺激开关的开发,极大地推动了精准治疗领域的发展,为克服现有治疗的局限性提供了新的策略。这些内源性刺激开关的开发,为克服现有治疗的局限性提供了新的策略和方法。 外源性刺激开关 外源性刺激开关是用外部物理信号实现药物的精准控制释放。例如,光刺激开关通过特定波长的光照触发药物释放,具有非接触性和精准时空控制的优势,尤其适用于需要局部治疗的场景。电场刺激开关则借助电场的方向和强度变化,精确调控药物释放的时间和位置,展现出良好的可控性和实时性。温度刺激开关结合外部热源与温度敏感材料,通过升高局部温度实现药物释放,这种方法具有良好的组织穿透性和热响应性。磁场刺激开关利用磁场的非侵入性和导向性,将磁性药物载体引导至目标区域,实现药物的定点递送和控释。超声刺激开关则利用超声设备产生的微小振动或空化效应,促进药物载体释放药物,具有良好的生物安全性和组织穿透能力。这些外源性刺激开关技术的发展,为药物递送提供了更加多样化和精准化的手段。 控释机制 可控释放机制可以实现药物的长效、稳定释放,减少给药频率,简化治疗方案。部位特异性释放机制通过靶向递送系统,使药物在指定部位富集,减少全身副作用。例如,利用壳聚糖(CS)的pH敏感性和二硫键的还原氧化敏感性设计的纳米粒子,可精准递送药物至肿瘤组织或细菌感染部位。速率特异性释放机制通过控制药物释放速率,模拟体内代谢过程,维持稳定疗效。例如,PNIPAM等温度敏感水凝胶能在特定温度下控制药物释放,而pH敏感聚合物则可在肿瘤微环境中缓慢释放药物。时间特异性释放机制则依据疾病特点和治疗需求,在特定时间释放药物。例如,基于生物可降解微粒的系统,可在数天至数周内实现药物的定时释放。这些机制为个性化医疗提供了技术支撑,显著提升了治疗效果并降低了副作用,推动了精准治疗领域的发展。 作者简介 王则君,东北大学理学院教授,博士生导师。国家级优秀青年人才、“兴辽英才计划”青年拔尖人才和沈阳市中青年科技创新人才。主要从事微纳诊疗器件与材料的设计、微液滴操控等方向的研究。课题组简介:http://faculty.neu.edu.cn/wangzejun/zh_CN/index.htm 文章信息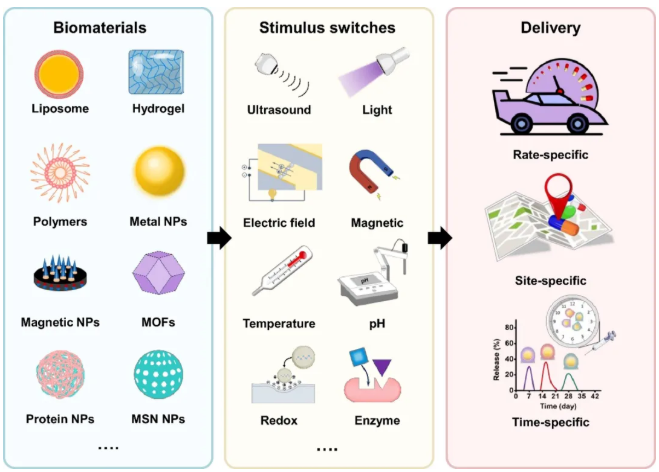

如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























































 京公网安备 11010802027423号
京公网安备 11010802027423号