龙亚秋团队JMC | 一箭三雕:靶向性、可视化和治疗干预于一体的生物正交多功能小分子骨架,实现活体内精准靶向药物释放与实时监测
英文原题:Novel Bioorthogonal Theranostic Scaffold Enables on-Target Drug Release and Real Time Monitoring In Vivo 通讯作者:龙亚秋(苏州大学) 作者:Jing Pang#, Shun Feng#, Bin Huang#, Jujun Zhou, Linjun Zhan, Ya-Qiu Long*
诊疗一体化(theranostics),是将目前临床上诊断和治疗两个分离的过程/功能组合在一个分子系统里,发挥早期诊断、影像引导治疗和预后评估等作用,是精准医学的重要技术支撑。然而,大多数已报道的诊疗一体化平台为多组分的纳米递送体系,存在成本高、重现性差和定量困难等问题,限制其进一步临床应用。近年来蓬勃发展的生物正交化学,以其高选择性、快速反应动力学和生物相容性等特点为时空可控精准诊疗提供强有力的手段。基于生物正交反应在病灶位激活的成像或/和治疗小分子药物,具有明确的分子结构和作用机制,并具有良好药代动力学性质和安全性,具有可转化潜力。但是靶向性的诊疗一体化小分子架构,通过一次生物正交反应触发产生多种功能,实现“一石三鸟”(靶向、成像和治疗)的效果,仍然是一个临床迫切需要却充满挑战的精准诊疗新模式(图1简示)。
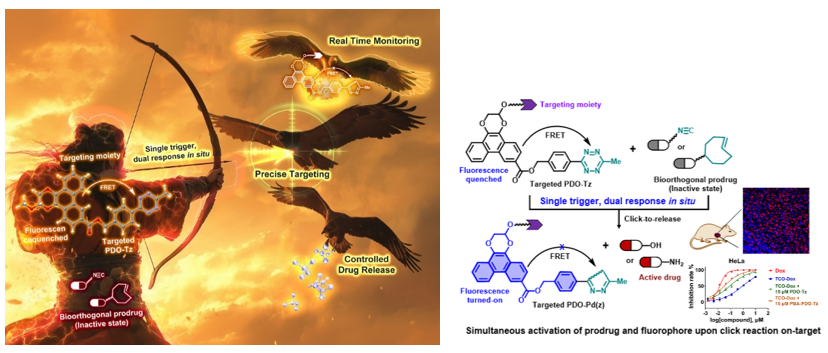
图1. 一箭三雕:新型多功能单一小分子骨架,经单次生物正交点击反应,激发精准诊疗、实时监测多重功效
为此,苏州大学龙亚秋教授(点击查看介绍)团队创制了一种全新结构的多功能分子骨架,能够通过生物正交点击反应实现在靶按需的药物释放和实时成像(如图1所示)。这一设计将治疗和诊断整合于单个小分子骨架,通过单次点击反应同时激活荧光发射和药物分子释放,并实现对肿瘤细胞的高选择性杀灭和实时监测。如图2所示,本研究首次将一种新的荧光发色团——菲并二噁英(phenanthrodioxine, PDO),与荧光屏蔽基团四氮唑(tetrazine, Tz)共缀,得到的 PDO-Tz 分子骨架因FRET效应而不具荧光。PDO-Tz 一旦遇到生物正交反应对基团所偶联的前药,旋即触发 Tz 介导的生物正交点击-释放反应,Tz 结构转化而丧失FRET效应,从而淬灭效应终止而恢复PDO的荧光并同时释放药物。值得一提的是,PDO 和 Tz 的 FRET 效应是首次在本研究中被观察并被应用于荧光开关;而且,在这个多功能骨架中,Tz 基团作为荧光团和药物活化的双重开关。另一方面,PDO 的构建来源于 9,10-菲醌(9,10-phenanthrenequinone, PQ)与可结构衍生化的富电子烯烃之间的光引发环加成反应,反应简单、快速而高产率,赋予了靶向配体可经烯烃分子方便高效地引入到 PDO-Tz 骨架上的能力,进而获得靶向性PDO-Tz骨架可以定位到特定的细胞器或细胞内蛋白质,实现精确的治疗干预和靶蛋白可视化。
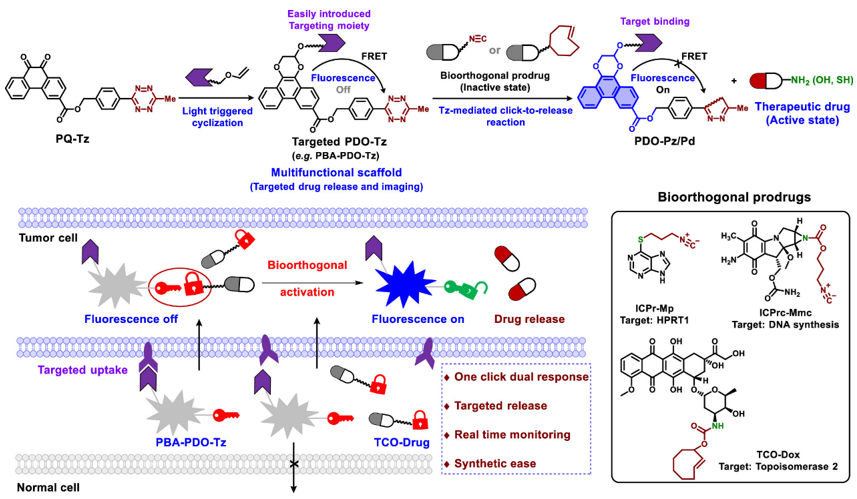
图2. “一石三鸟”生物正交分子骨架的构建、作用原理以及生物正交前药的结构
在概念验证研究中,作者创制的这一新颖生物正交诊疗骨架,成功应用于反式环辛烯偶联的抗癌药物阿霉素(trans-cyclooctene-caged Doxorubicin, TCO-Dox)在活细胞里的荧光成像和原药释放,荧光开关比率接近44倍。而且,恢复发射的荧光强度与药物释放浓度呈线性关系,使得精准、实时和定量监测药物释放成为可能。同时,阿霉素的前药 TCO-Dox 被 PDO-Tz 点击释放后恢复了对A549肺癌细胞的强效杀伤活性。进一步引入苯硼酸 (phenylboronic acid, PBA)靶向基团的诊疗一体化骨架 PBA-PDO-Tz,因为 PBA 能识别肿瘤细胞高表达的唾液酸残基,所以确保了 PBA-PDO-Tz 的肿瘤细胞选择性富集,进一步引发了 TCO-Dox 在肿瘤细胞的荧光成像和靶向性细胞毒性(如图3所示)。特别有意义的是,PBA-PDO-Tz 的体内靶向药物释放和实时成像功能在小鼠的A549肿瘤移植模型上得到了验证(如图3所示)。加之合成易得性,该生物正交多功能小分子骨架提供了一个富有转化医学前景的诊疗一体化平台,将有助于开发新型诊疗一体化模式用于肿瘤的精准诊断、治疗、预后和实时监测。
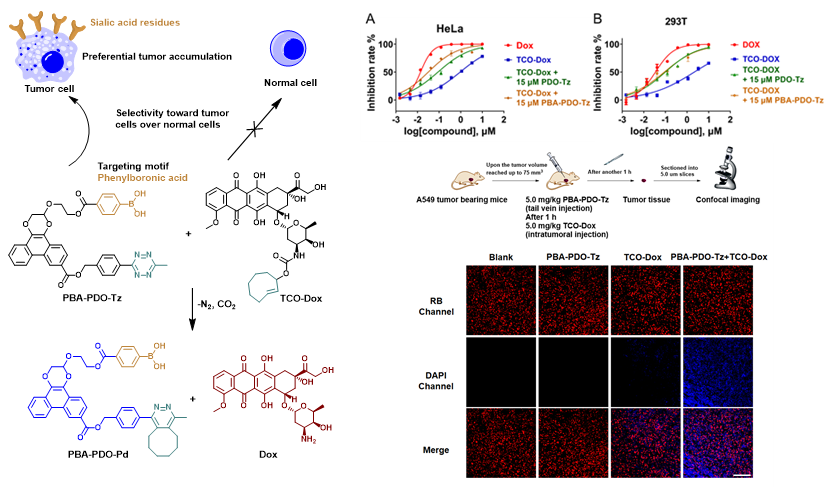
图3. 肿瘤细胞靶向性多功能分子骨架 PBA-PDO-Tz 引发选择性细胞毒性及其小鼠移植瘤模型的瘤内成像
该成果近期发表于Journal of Medicinal Chemistry,文章的通讯作者为苏州大学龙亚秋教授,第一作者为苏州大学博士生庞京、封顺和副教授黄斌。该研究工作得到了国家自然科学基金 (22377088, 81903442)、苏州市科技发展计划(关键核心技术“揭榜挂帅”攻关)项目(SYG2024147)、苏州医学院基础前沿创新交叉科研专项医学交叉种子基金(YXY2304077)的资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Novel Bioorthogonal Theranostic Scaffold Enables on-Target Drug Release and Real Time Monitoring In Vivo
Jing Pang#, Shun Feng#, Bin Huang#, Jujun Zhou, Linjun Zhan, Ya-Qiu Long*
J. Med. Chem. 2025, 68, 3, 3824–3836
https://doi.org/10.1021/acs.jmedchem.4c02965
Published January 31, 2025
Copyright © 2025 American Chemical Society
(本稿件来自ACS Publications)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!













































 京公网安备 11010802027423号
京公网安备 11010802027423号